Limbus reaction following scleral lens fitting
Purpose. To investigate quadrant-specific changes in limbal tissue thickness after 7 days of scleral lens wear using anterior segment OCT (AS-OCT), and the associated changes in central corneal thickness (CCT), central epithelial thickness (CET), and central corneal clearance (CCC).
Material and Methods. In this observational study, 20 eyes of 11 scleral lens neophytes (35 ± 12 years; 4 eyes with keratoconus) were fitted with a scleral lens. CCT and CET were measured with a swept-source AS-OCT system; limbal tissue thickness was determined in four quadrants at three locations each, and CCC was documented. Two baseline measurements on different days before lens wear and one measurement after 7 days of daily wear (≥ 8 h/day) were performed. Changes were analysed descriptively.
Results. After 7 days, CCT increased from 525.75 ± 55.24 µm to 537.48 ± 58.53 µm (Δ +11.73 µm), while CET remained unchanged from 51.31 ± 9.19 µm to 51.03 ± 9.03 µm (Δ −0.28 µm). The limbal area showed a quadrant-specific pattern: thickening up to +20.9 µm nasally, +32.3 µm temporally and +50.3 µm inferiorly contrasted with thinning up to −56.7 µm superiorly. CCC decreased from 288.4 ± 61.7 µm to 232.2 ± 56.0 µm (Δ −56.1 µm).
Conclusion. Seven days of scleral lens wear are associated with quadrant-specific changes in limbal tissue thickness, a small increase in CCT, stable CET and a moderate reduction in CCC, supporting limbal thickness as a potentially early-responding structural parameter under scleral lenses.
Einführung
Only the abstract of the article "Limbus reaction following scleral lens fitting" is available in English. The complete article can be read in German.
Sklerallinsen haben sich in den vergangenen Jahren als wichtige Versorgungsoption für Patient*innen mit irregulären Hornhautoberflächen, komplexen refraktiven Situationen und ausgeprägten Benetzungsstörungen etabliert.1,2,3 Im Vergleich zu kornealen formstabilen Linsen überbrücken sie Kornea und Limbus vollständig und liegen ausschließlich auf der Sklera auf.1,2 Zwischen Linsenrückfläche und Hornhaut entsteht ein geschlossenes Tränenreservoir, das optische Irregularitäten neutralisiert und zugleich einen mechanischen Schutz des Epithels bietet.1,2,3
Diese Kontaktlinsengeometrie führt jedoch zu spezifischen, physiologischen Herausforderungen. Die avaskuläre Kornea ist auf eine ausreichende Sauerstoffversorgung über Umgebungsluft, Tränenfilm, Kammerwasser und peripher limbal diffundierende Gefäße angewiesen.4 Ein zusätzliches Flüssigkeitsreservoir und die Linsendicke erhöhen den Diffusionswiderstand und können, insbesondere bei längerer Tragedauer oder ungünstiger Geometrie, zu hypoxieinduzierten Ödemen führen.5,6,7,8 Parallel wirken mechanische Kräfte an der skleralen Auflagezone, die sich bis in den limbusnahen Bereich der Kornea fortsetzen können.9,10,11
Der Limbus nimmt hierbei eine Schlüsselrolle ein. Er beherbergt epitheliale Stammzellnischen, die für die Regeneration des Korneaepithels essenziell sind.12,13,14 Eine chronische Überlastung durch Hypoxie oder mechanische Irritation kann zur limbalen Stammzellinsuffizienz (limbal stem cell deficiency, LSCD) mit Neovaskularisation, konjunktivaler Epithelmigration und epithelialer Instabilität führen.15,16,17 Klinisch relevante LSCD-Formen wurden wiederholt mit langjährigem Kontaktlinsentragen in Verbindung gebracht.18
Mehrere Kurzzeitstudien beschreiben morphologische und topografische Veränderungen von Konjunktiva, Episklera und Sklera bereits nach wenigen Stunden Sklerallinsentragezeit.10,11 Systematische Daten zu quadranten-spezifischen Veränderungen der limbusnahen Gewebedicke unter alltagsnahen Tragebedingungen sind jedoch rar. Ein expliziter Bezug zwischen zentraler Hornhautdicke (CCT), zentraler Epitheldicke (CET), limbusnaher Gewebedicke und zentraler kornealer Überbrückung (central corneal clearance, CCC) über mehrere Tage Tragedauer ist bislang nur unzureichend beschrieben.19,20,21
Ziel der Studie war es daher, mittels hochauflösender Swept-Source-Vorderabschnitts-OCT quadranten-spezifische Veränderungen der limbusnahen Gewebedicke nach sieben Tagen Sklerallinsen-Tragezeit zu erfassen und diese mit Veränderungen von CCT, CET und CCC in Beziehung zu setzen. Im Sinne einer explorativen Hypothese wurde erwartet, dass der Limbus eine ausgeprägte Dickenänderung zeigt, während CCT und CET nur geringfügig beeinflusst werden.
Material und Methoden
Studiendesign
Es handelt sich um eine nicht-interventionelle, prospektive, einarmige Beobachtungsstudie (Fallserie), welche im Kontaktlinseninstitut Wörle in München durchgeführt wurde. Untersucht wurden strukturelle Anpassungsreaktionen des vorderen Augenabschnitts nach sieben Tagen Tragezeit von Sklerallinsen unter üblichen Alltagsbedingungen.
Probandinnen
In die Studie wurden elf erwachsene Proband*innen
(20 Augen; Alter 35 ± 12 Jahre) eingeschlossen. Die Mehrzahl der Augen wies eine reguläre Kornea auf, bei vier Augen bestand ein diagnostizierter Keratokonus.
Einschlusskriterien waren unter anderem die Eignung für eine Sklerallinsenversorgung, stabile okuläre Verhältnisse und die Bereitschaft, die Linsen über sieben Tage täglich mindestens acht Stunden zu tragen. Ausgeschlossen wurden aktive entzündliche Erkrankungen des vorderen Augenabschnitts, ausgeprägte Trockenheit, relevante Lidpathologien sowie systemische Erkrankungen mit potenziellem Einfluss auf die Kornea. Zudem gab es eine vorgeschriebene Kontaktlinsenkarenz im Vorfeld der Studie (30 Tage).
Alle Studienteilnehmer waren Sklerallinsen-Neuträger*innen. Sie wurden über Ziel, Ablauf und mögliche Risiken der Untersuchung informiert und gaben hierzu ihre schriftliche Einwilligung. Die demografischen und okularen Ausgangsdaten sowie die wesentlichen Anpassparameter wurden anonymisiert zusammengefasst.
Kontaktlinsen
Alle Augen wurden mit individuell angepassten Sklerallinsen des Typs Zenlens (Bausch + Lomb, USA) versorgt. Es handelt sich um moderne Sklerallinsen in vier verfügbaren Durchmessern von 14,8 - 17,0 mm mit hochsauerstoffdurchlässigen Materialien (Dk > 100).22
Das Design umfasst:
• eine zentrale optische Zone, welche die Kornea mit einem geschlossenen Tränenreservoir überwölbt und den refraktiven Fehler korrigiert,
• eine limbale Übergangszone, die den Limbus überbrückt und mechanische Belastung der Stammzellnischen reduzieren soll,
• eine sklerale Auflagezone, die sphärisch oder torisch gestaltet werden kann, um der individuellen Sklerageometrie zu entsprechen.22,23
Die Wahl der ersten Anpasslinse erfolgte anhand sagittaler Tiefe und horizontal sichtbarem Irisdurchmesser. Ziel war eine initiale CCC von circa 250 - 350 µm unmittelbar nach Aufsetzen der Linse, unter Berücksichtigung eines erwarteten Senkungs-Effekts von 100 - 150 µm.22
Messinstrumente
Die morphologischen Messungen wurden mit einem Swept-Source-Vorderabschnitts-OCT-System (Anterion, Heidelberg Engineering, Deutschland) durchgeführt. Das System arbeitet mit einer Wellenlänge von 1300 nm und bietet eine axiale Auflösung von circa 10 µm bei einer Eindringtiefe bis 6 mm.24 Alle Messungen erfolgten nach identischem Protokoll und möglichst zur gleichen Tageszeit, um tageszeitliche Schwankungen zu minimieren.
Das Vorgehen zur Definition der limbalen Messpunkte ist in Bild 1 schematisch dargestellt.
Die klinische Beurteilung von zentraler, sowie limbaler Überbrückung und skleraler Auflage erfolgte mit Spaltlampe und Fluoreszein. Bei ausgeprägter Asymmetrie der Sklera wurden torische Rückflächendesigns gewählt, um eine gleichmäßige Auflage der Linse zu gewährleisten.23
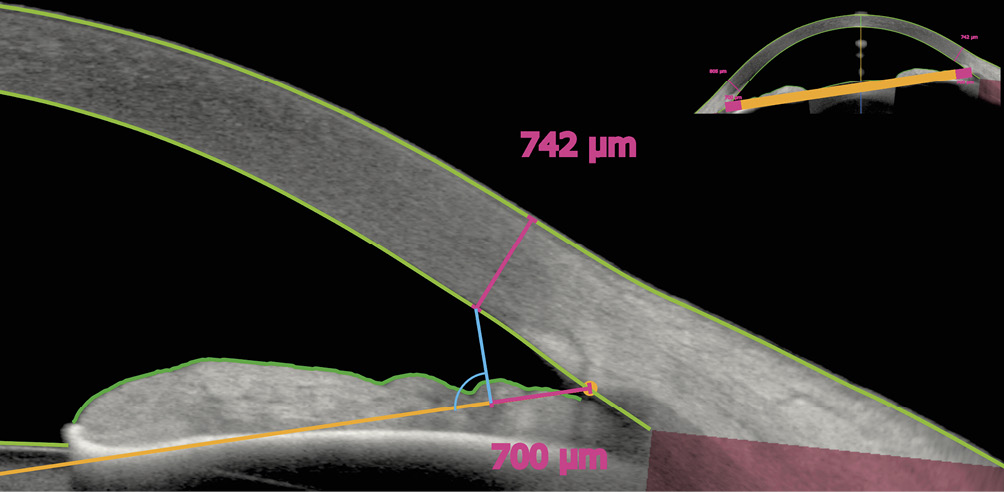
Bestimmung der limbalen Messpunkte und Reproduzierbarkeit
Als anatomische Referenz diente die vom Anterion automatisch detektierte Skleralsporn-zu-Skleralsporn-Linie. Ausgehend von jedem Skleralsporn wurden in jedem Quadranten (nasal, temporal, superior, inferior) Messpunkte in 500, 600 und 700 µm Abstand in Richtung Hornhautzentrum definiert. Von diesen Punkten wurde jeweils eine Orthogonale zur Sporn-zu-Sporn-Achse konstruiert und bis zur posterioren Hornhautoberfläche projiziert. Die limbusnahe Gewebedicke wurde am definierten Messort als Abstand zwischen anteriorer und posteriorer Grenzfläche senkrecht zur anterioren Oberfläche bestimmt.3
Der Skleralsporn (Anterion-Autodetektion) diente ausschließlich als stabiler Positionsanker; zur Plausibilitätskontrolle wurde zusätzlich die Sporn-zu-Sporn-Distanz dokumentiert.25,26
Zur Beurteilung der Wiederholgenauigkeit wurden bei einer Probandin fünf aufeinanderfolgende Messreihen an beiden Augen erhoben und der Wiederholbarkeits-Koeffizient (Repeatability Coefficient) (RC, 95 %) berechnet: RC = 6,66 µm (700 µm) < 7,38 µm (600 µm) < 8,53 µm (500 µm). Damit nahm die Reproduzierbarkeit mit zunehmender Nähe zum Skleralsporn leicht ab, wahrscheinlich bedingt durch optische Inhomogenitäten im Übergangsbereich zwischen Kornea und Sklera. Die RC-Werte lagen deutlich unter den im Gesamtkollektiv beobachteten limbalen Veränderungen von bis zu ±50 µm. Differenzen um circa 10 µm wurden als methodennah interpretiert, größere Änderungen als wahrscheinliche Anpassungsreaktion gewertet.27
Messzeitpunkte und Trageprotokoll
Das Untersuchungsprotokoll umfasste folgende Zeitpunkte:
• T0: Baseline vor Anpassung (ohne Sklerallinsen)
• T1: Re-Baseline an einem separaten Tag (ohne Sklerallinsen)
• C1: CCC-Messung 20 Minuten nach Aufsetzen der final angepassten Sklerallinse
• Tägliche Tragephase: 7 Tage, jeweils ≥ 8 h/Tag unter Alltagsbedingungen
• C2: CCC-Messung nach 7 Tagen, am Ende eines Tragetages (mit Sklerallinse)
• T2: Abschlussmessung von CCT, CET und limbusnaher Gewebedicke (ohne Sklerallinse), ≤ 10 Minuten nach Linsenabnahme
Datenverarbeitung und Statistik
Die Auswertung erfolgte deskriptiv. Ergebnisse werden als Mittelwert ± SD sowie als Δ-Werte berichtet. Aufgrund der bilateralen Messungen ohne Adjustierung für intraindividuelle Abhängigkeiten werden keine inferenzstatistischen Kennwerte angegeben. Die Interpretation orientiert sich daher primär an Effektgrößen und der Konsistenz der quadrantenspezifischen Muster.
Ethische Aspekte
Die Beobachtungsstudie wurde im Rahmen der regulären Kontaktlinsenversorgung von 11 Patient*innen (20 Augen) im Kontaktlinseninstitut Wörle (München) durchgeführt. Die Studie erfolgte in Übereinstimmung mit der Deklaration von Helsinki sowie unter Berücksichtigung der Europäischen Datenschutz-Grundverordnung (DSGVO) und der einschlägigen Richtlinien der Hochschule München. Von allen Patient*innen wurde eine schriftliche Einwilligung zur Verarbeitung und wissenschaftlichen Auswertung der pseudonymisierten Daten eingeholt.
Ergebnisse
Baseline-Reproduzierbarkeit
Zwischen den beiden Baseline-Messungen (T0, T1) zeigten sich für die zentrale Hornhautdicke (CCT: 525,42 ± 54,53 µm vs. 526,08 ± 55,95 µm) und die zentrale epitheliale Dicke (CET: 51,58 ± 9,97 µm vs. 51,03 ± 8,40 µm) keine systematischen Unterschiede; die Absolutdifferenzen lagen jeweils < 1 µm. Auch die limbalen Messpunkte waren insgesamt stabil, mit sehr geringen Mittelwertdifferenzen zwischen T0 und T1. Kleine Mittelwertdifferenzen traten bei nasal 500 µm (Δ = +4,05 µm), temporal 600 µm (Δ = +1,18 µm) sowie superior 700 µm (Δ = +1,04 µm) auf und wurden aufgrund der geringen Absolutdifferenzen als Messvariabilität im Rahmen multipler Vergleiche interpretiert. Insgesamt stützen die Ergebnisse die hohe Reproduzierbarkeit der Messmethode und rechtfertigen die Verwendung des Mittelwerts aus T0 und T1 als Baseline für die Verlaufsanalyse.
Zentrale Hornhautdicke (CCT) und zentrale Epitheldicke (CET)
Wie in Tabelle 1 dargestellt, stieg die zentrale Hornhautdicke nach sieben Tagen Tragezeit um Δ = +11,73 µm, während die zentrale epitheliale Dicke nahezu unverändert blieb (Δ = −0,28 µm). Damit zeigen die Ergebnisse eine geringe, aber konsistente zentrale Verdickung der Kornea um 2,2 %, ohne begleitende zentrale epitheliale Anpassung im untersuchten Zeitraum.
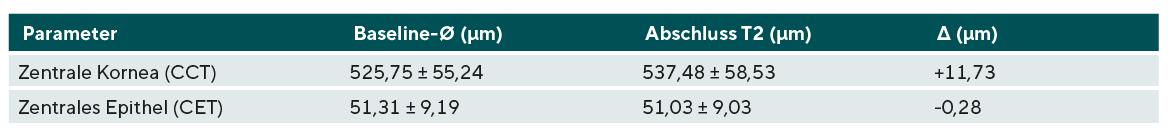
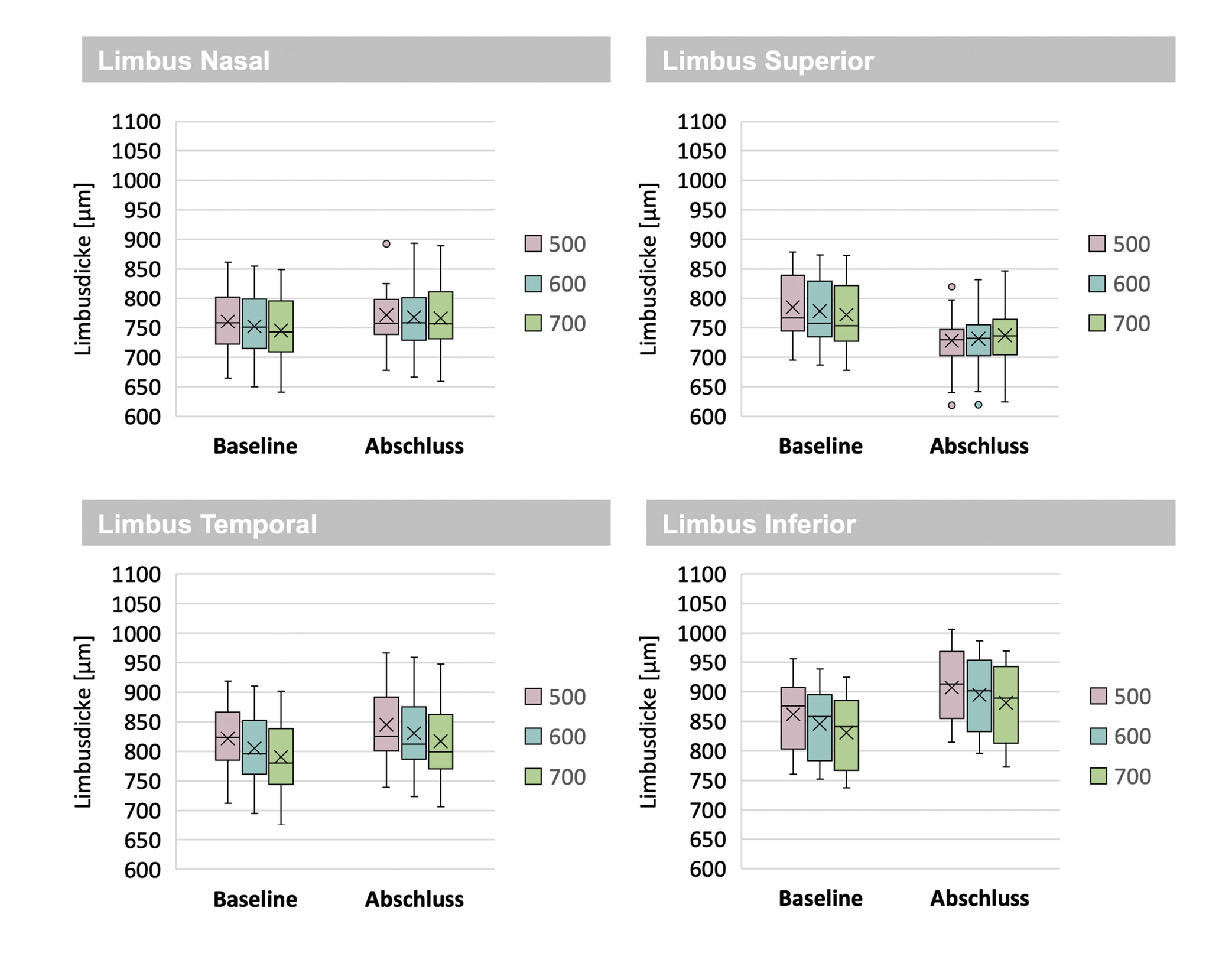
Limbus
Wie in Bild 2 dargestellt, zeigte sich nach sieben Tagen Sklerallinsen-Tragezeit ein ausgeprägt quadrantenspezifisches Muster der limbusnahen Gewebedicke. Im nasalen Quadranten nahm die Dicke an allen Messabständen zu, wobei die stärkste Zunahme bei 700 µm auftrat (Δ = +20,9 µm). Auch temporal zeigte sich eine konsistente Verdickung an allen Messpunkten; am deutlichsten war der Effekt bei 500 µm (Δ = +32,3 µm).
Demgegenüber kam es im superioren Quadranten zu einer Abnahme der Gewebedicke über alle Abstände, mit der größten Reduktion bei 500 µm (Δ = −56,7 µm). Im inferioren Quadranten zeigten sich ebenfalls an allen Messabständen Zunahmen, mit dem stärksten Effekt bei 700 µm
(Δ = +50,3 µm).
Über alle Abstände zeigte sich konsistent: superior ↓ (bis −56,7 µm) und inferior ↑ (bis +50,3 µm), mit moderater Zunahme nasal (bis +20,9 µm) und temporal (bis +32,3 µm). Die Boxplots verdeutlichen dieses stabile, quadrantenspezifische Muster (Verdickung nasal/temporal/inferior, Verdünnung superior).
Zentrale korneale Überbrückung (CCC)
Die CCC verringerte sich von 288,4 ± 61,7 µm (C1) auf 232,2 ± 56,0 µm (C2). Dies entspricht einer mittleren Abnahme von 56,1 µm. Der Endwert lag mit 232 µm im empfohlenen Zielbereich von 150 - 250 µm laut Zenlens-Fitting-Guide.22
Diskussion
Die vorliegende Beobachtungsstudie zeigt, dass unter kurzzeitigem Sklerallinsentragen nicht die zentrale Kornea, sondern vor allem der Limbus die ausgeprägtesten strukturellen Veränderungen aufweist. Die zentrale Aussage beruht dabei weniger auf Einzelmesspunkten als auf der reproduzierbaren Richtung und Größenordnung der Veränderungen über Quadranten und Messabstände. Diese zeigen eine klare Konsistenz in Richtung und Effektgröße, mit superiorer Ausdünnung und deutlicher Dickenzunahme inferior.
Einordnung und mögliche Mechanismen
Kurzzeitstudien konnten zeigen, dass Sklerallinsen bereits nach wenigen Stunden zu Form- und Höhenveränderungen an Konjunktiva, Episklera und Sklera führen, wobei insbesondere superior betonte Kompressions- und Abflachungseffekte beschrieben wurden.10,11 Dies passt zu der hier gemessenen superioren Ausdünnung der limbusnahen Gewebedicke und stützt die Interpretation, dass in diesem Bereich vor allem eine mechanische Kompression dominiert. Neben der Geometrie, der skleralen Auflagezone, wirken die Kräfte des Oberlids, welches die Linse beim Lidschlag wiederholt gegen die obere Sklera drückt und damit im Übergangsbereich zwischen optischer Zone, limbaler Zone und Haptik einen ausgeprägten Druckgradienten erzeugen kann.9-11 Die stärksten Effekte nahe dem Skleralsporn sprechen dafür, dass gerade diese Übergangsregion biomechanisch besonders sensibel ist.
Die inferioren Verdickungen sind demgegenüber plausibel als Ausdruck von Gewebequellung zu interpretieren. Unter Sklerallinsen ist bekannt, dass Materialeigenschaften, Linsendicke und Höhe des Tränenreservoirs die Sauerstofftransmission begrenzen und bei unzureichender Versorgung stromale Ödeme begünstigen können.5,6,7,8,19,21 Modellierungen und experimentelle Daten zeigen, dass zentrale und periphere Hornhautverdickungen auftreten können, wenn der Sauerstoffpartialdruck unter kritische Schwellen sinkt.6,7,19,21 Die zentrale Zunahme der Hornhautdicke von etwa 2 % ordnet sich in diesen Rahmen ein und bleibt unterhalb der häufig diskutierten 4 %-Grenze klinischer Relevanz.5,7,8 Auf den limbusnahen Bereich übertragen ist denkbar, dass regional erhöhte Überbrückung, geringgradige Dezentrierung und gravitationsbedingte Flüssigkeitsansammlung inferior zu einem Ungleichgewicht aus mechanischer Entlastung und hypoxischer Belastung führen und damit eine lokale ödematöse Verdickung begünstigt.6,9,19,20,22
Die moderaten, aber konsistenten Verdickungen in den nasalen und temporalen Quadranten des Limbus lassen sich als Mischbild aus mechanischer Belastung und hypoxischer Gewebeantwort interpretieren.9,10,11 Dass die Richtung der Veränderung innerhalb jedes Quadranten über alle Messabstände stabil bleibt und die beobachteten Differenzen deutlich über der methodischen Variabilität liegen, spricht gegen zufällige Messartefakte und für ein anatomisch verankertes Reaktionsmuster. Auch im Vergleich zur Messwiederholgenauigkeit (RC ≈ 7 - 9 µm) liegen die beobachteten Maximaländerungen (bis ±50 µm) deutlich darüber. Die stabile zentrale Epitheldicke steht im Einklang mit Untersuchungen, die bei Kurzzeit-Tragen primär stromale Ödeme nachweisen und in Langzeitbeobachtungen unter gut angepassten Sklerallinsen keine relevanten zentral-epithelialen Remodellierungen beschreiben, und legt nahe, dass in dem untersuchten Zeitfenster vor allem stromale und limbusnahe Strukturen beeinflusst werden, während sich das zentrale Epithel vergleichsweise robust zeigt.19,21
Limbusdicke als früh reagierender Strukturparameter
Der Limbus beherbergt die Stammzellnischen des Korneaepithels, die für die kontinuierliche Regeneration und Homöostase der Hornhautoberfläche verantwortlich sind.12-17 Die Palisaden von Vogt gelten als morphologisches Korrelat dieser Stammzellareale und als Schlüsselstruktur für die Integrität der Hornhautoberfläche.12,14,28 Störungen in diesem Bereich, etwa durch chemische oder thermische Insulte, chronische Entzündungen, immunvermittelte Erkrankungen oder langjähriges Kontaktlinsentragen, können in eine limbalen Stammzellinsuffizienz (LSCD) münden, die mit persistierenden Epitheldefekten, Neovaskularisation, stromalen Trübungen und Visusverlust einhergeht.12-16,18,21,28 Kontaktlinsenassoziierte LSCD wurde in einer größeren Fallserie als relevante klinische Entität beschrieben und auch bei systemischen Erkrankungen mit ausgeprägter okulärer Oberflächenbeteiligung, wie der okulären Graft-versus-Host-Erkrankung (oGvHD), werden limbusbezogene Schäden als zentraler Mechanismus diskutiert.16,18
Vor diesem Hintergrund erscheint die limbusnahe Gewebedicke als potenziell interessante strukturelle Kenngröße, die frühe Anpassungsreaktionen im Bereich der Stammzellnischen erfassen könnte. Die vorliegenden Ergebnisse zeigen, dass sich unter klinisch unauffälligen Kurzzeitbedingungen bereits nach einer Woche reproduzierbare, quadrantenspezifische Veränderungen objektivieren lassen. Ob diese Veränderungen prognostische Relevanz für spätere klinische Komplikationen besitzen, hängt jedoch nicht nur von ihrem Ausmaß, sondern entscheidend von ihrer Dynamik nach Linsenabnahme ab. Solange unklar ist, wie rasch sich die beobachteten Verdickungen und Ausdünnungen nach Absetzen der Linse zurückbilden, bleibt offen, ob es sich primär um reversible, physiologische Anpassungsreaktionen oder um potenziell persistierende Vorläufer struktureller Schädigungen handelt.
In der vorliegenden Beobachtungsstudie wurde der zeitliche Verlauf nach Linsenabnahme nicht untersucht; Messungen erfolgten erst nach vollständiger Tragewoche und nicht in definierten Intervallen in der Regenerationsphase ohne Linse. Aussagen zur Reversibilität, zur Erholungszeit und zu möglichen kumulativen Effekten bei längerer Tragedauer sind daher nicht möglich. Gerade diese Parameter wären jedoch entscheidend, um die prognostische Aussagekraft der Limbusdicke zu prüfen. Ein rasch und vollständig reversibler Befund hätte eine andere prognostische Bedeutung als persistierende Veränderungen, die auch nach Tragepausen nachweisbar bleiben.
Die Ergebnisse legen nahe, den Limbus bei zukünftigen Sklerallinsenstudien gezielt als früh reagierendes Organ zu betrachten und limbusnahe Dickenmessungen mit Vorderabschnitts-OCT in longitudinalen Designs zu prüfen. Besonders informativ wären Studien, die sowohl den Verlauf unter kontinuierlichem Tragen als auch die Regeneration nach definierten Tragepausen untersuchen und diese strukturellen Verläufe mit klinischen Endpunkten wie LSCD-Zeichen, oGvHD-assoziierten Oberflächenveränderungen oder stromalen Trübungen verknüpfen.12-16,18,21,28
Klinische Bedeutung
Die Ergebnisse verdeutlichen, dass Anpassungsreaktionen unter Sklerallinsen nicht auf die zentrale Hornhaut beschränkt sind, sondern sich frühzeitig und deutlich ausgeprägter perilimbal manifestieren können. Für die klinische Praxis bedeutet dies, dass neben der Beurteilung der zentralen Hornhautüberbrückung und der zentralen Hornhautdicke, insbesondere die limbalen Übergangsbereiche sowie die sklerale Auflagezone systematisch beurteilt werden sollten.1,2,3,9,22,23 Superior ist dabei auf Zeichen übermäßiger Kompression zu achten, etwa Blanching, Einschnürungen oder segmentale Injektionen nach Linsenabnahme, während inferior eher Hinweise auf ödematöse Belastung und vermehrtes Fogging Beachtung finden sollten.1,9,10,22
Die Vorderabschnitts-OCT kann die Spaltlampenuntersuchung ergänzen, indem sie eine objektive und reproduzierbare Quantifizierung von limbusnahen Gewebedicken und Überbrückung ermöglicht.24,29 So lassen sich auch subtile Veränderungen dokumentieren, die klinisch nur schwer sichtbar sind. Verläufe der limbusnahen Dicke können genutzt werden, um den Effekt von Designmodifikationen, etwa Anpassungen der limbalen Zone, Variation der sagittalen Höhe oder Einsatz torischer bzw. quadrantenspezifischer Haptiken, zu evaluieren und Quadranten gezielt zu entlasten, die eine ausgeprägte Reaktion zeigen.9,22,23,29
Besonders bei Patient*innen mit erhöhtem Risiko für Oberflächenkomplikationen, etwa nach vorausgegangenen Hornhauterkrankungen, bei bestehenden limbalen Auffälligkeiten oder im Rahmen systemischer Grunderkrankungen mit signifikanter okulärer Oberflächenbeteiligung, wie der okulären Graft-versus-Host-Erkrankung, erscheint eine frühe und engmaschige Überwachung des Limbus sinnvoll.12-16,18,21,28 Auch wenn aus der vorliegenden Arbeit keine direkten Aussagen zu Langzeitfolgen abgeleitet werden können, unterstreichen die gezeigten limbalen Strukturveränderungen die Notwendigkeit, diesen Bereich in der Anpassung und Nachsorge von Sklerallinsen ausdrücklich zu berücksichtigen.
Limitationen und Ausblick
Die Interpretation der Ergebnisse ist durch die begrenzte Stichprobengröße und die heterogene Zusammensetzung der Gruppe mit überwiegend gesunden Augen und vier Keratokonus-Augen eingeschränkt. Eine differenzierte Subgruppenanalyse war nicht möglich, sodass keine belastbaren Aussagen zu potenziellen Unterschieden zwischen diesen Entitäten getroffen werden können. Dies führt ebenso dazu, dass die Anpassreaktionen nicht uneingeschränkt auf beide Gruppen übertragbar sind. Die Auswertung erfolgte auf Augenebene ohne Adjustierung für intraindividuelle Abhängigkeiten, sodass die Ergebnisse primär deskriptiv-explorativ zu interpretieren sind. Alternativ könnte in zukünftigen Studien zur Sicherung statistischer Unabhängigkeit nur ein Auge pro Person analysiert werden. Zudem wurden mehrere Quadranten und Messabstände untersucht, die Ergebnisse sind daher deskriptiv auszuwerten, die Interpretation sollte sich in erster Linie an der Konsistenz der Muster und der Größenordnung der Effekte orientieren.27
Der Beobachtungszeitraum von sieben Tagen erlaubt nur eine Kurzzeitbetrachtung. Es bleibt offen, ob sich die beobachteten limbalen Veränderungen unter fortgesetztem Tragen stabilisieren, weiter zunehmen oder sich teilweise zurückbilden, und inwieweit sie mit klinisch relevanten Endpunkten wie LSCD-Zeichen, GvHD-assoziierten Oberflächenkomplikationen, Trübungen oder Visusminderung verknüpft sind.12-16,18,21,28 Zudem kann ohne die Nachverfolgung definierter Erholungsintervalle keine Aussage getroffen werden, ob die beobachteten Veränderungen vollständig reversibel sind oder potenziell kumulative Effekte darstellen. Funktionelle Parameter wie Sehleistung, Tragekomfort, Symptom-Scores oder Vitalfärbungen wurden nicht systematisch erfasst und konnten daher nicht mit den strukturellen Veränderungen korreliert werden.
Zukünftige Arbeiten sollten längere Beobachtungszeiträume, größere und homogene Kollektive sowie klar definierte klinische Endpunkte einbeziehen. Besonders sinnvoll erscheint die Kombination aus strukturellen limbusnahen Parametern, funktionellen Messgrößen und subjektiven Symptomen, ergänzt um Messungen in definierten Intervallen nach Linsenabnahme, um zu prüfen, ob sich charakteristische Muster limbaler Anpassungs- und Erholungsreaktionen identifizieren lassen, die als prädiktive Marker für spätere Komplikationen dienen können.
Fazit
Nach sieben Tagen Sklerallinsen-Tragezeit zeigte sich in dieser Studie eine geringe Zunahme der zentralen Hornhautdicke um +11,7 µm bei stabiler zentraler Epitheldicke, was für ein geringes, vorwiegend stromales Ödem ohne zentrale epitheliale Remodellierung spricht. Deutlich stärker reagierte der Limbus, wo ausgeprägte, quadrantenspezifische Veränderungen mit inferioren Verdickungen von bis zu +50,3 µm und superioren Ausdünnungen von bis zu −56,7 µm beobachtet wurden. Dieses Muster ist konsistent mit einem Zusammenspiel aus vorwiegend mechanischer Kompression im superioren Bereich und eher ödematös-physiologischen Effekten inferior. Klinisch sollte die Nachsorge unter Sklerallinsen daher nicht nur die zentrale korneale Überbrückung, sondern insbesondere die superioren und inferioren Auflage- und Übergangszonen systematisch einschließen; bei auffälligen limbalen Befunden sind gezielte Designanpassungen, etwa mittels torischer oder quadrantenspezifischer Haptiken und Modifikation der limbalen Zone, in Erwägung zu ziehen. Die beobachteten limbalen Strukturänderungen unterstreichen zudem, dass limbusnahe Dickenmessungen als potenziell früh reagierender struktureller Parameter in longitudinalen Studien weiter untersucht werden sollten.
Interessenkonflikt
Die Autoren haben keinen Interessenkonflikt in Bezug auf die im Artikel genannten Methoden und Geräte.
McMahon, T., Djalilian, A. (2016). Contact Lens-induced Limbal Stem Cell Deficiency. Ocul. Surf., 14, 419-434.
18 June 2025.